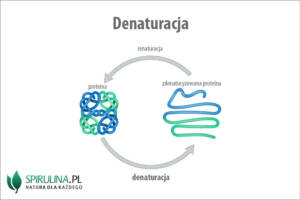
 Denaturacja to nieodwracalny proces, podczas którego struktura przestrzenna białka zostaje zniszczona. Zjawisko to może wywołać wiele czynników, takich jak np. wysoka temperatura czy etanol. W praktyce denaturację najlepiej zaobserwować można np. smażąc jajka na patelni, co powoduje widoczne gołym okiem ścinanie się białka wokół żółtka.
Denaturacja to nieodwracalny proces, podczas którego struktura przestrzenna białka zostaje zniszczona. Zjawisko to może wywołać wiele czynników, takich jak np. wysoka temperatura czy etanol. W praktyce denaturację najlepiej zaobserwować można np. smażąc jajka na patelni, co powoduje widoczne gołym okiem ścinanie się białka wokół żółtka.
Czym są białka?
Białka, czyli proteiny, są podstawowymi składnikami strukturalnymi wszystkich organizmów żywych, zarówno zwierzęcych, jak i roślinnych. To związki wielkocząsteczkowe, zbudowane z aminokwasów połączonych wiązaniem peptydowym. Ich masa cząsteczkowa przekracza 10000 daltonów (Da). Peptydy o niższej masie cząsteczkowej nazywane są oligopeptydami. Nie da się jednoznacznie określić budowy wszystkich białek, ponieważ jest ona niezwykle różnorodna i zależy od rodzaju białka.
Denaturacja – na czym polega?
Denaturacją nazywamy nieodwracalny proces, polegający na niszczeniu przestrzennej struktury II, III, i IV-rzędowej białek pod wpływem czynników fizycznych i czynników chemicznych. Do czynników fizycznych zaliczamy:
- ogrzewanie (wysokie temperatury) – dla niektórych białek wystarczy już temperatura 40 stopni C;
- silnie mieszanie i wytrząsanie – gwałtowne mieszanie czy ubijanie białka powoduje zerwanie wiązań wodorowych;
- naświetlanie promieniowaniem nadfioletowym (nazywanym również promieniowaniem UV), promieniowaniem rentgenowskim i promieniowaniem jonizującym;
- ultradźwięki.
Czynnikami chemicznymi są zaś:
- etanol – ma zdolność do przenikania przez ściany komórkowe bakterii i denaturacji obecnych w mikroorganizmach białek i enzymów, co prowadzi do śmierci komórki;
- mocznik;
- chlorek guanidyny;
- mocne kwasy i zasady – ulegają dysocjacji elektrolitycznej w roztworze rozpuszczalnika. W efekcie zaburzają one wiązania jonowe w mostkach solnych w białku, niszcząc jego strukturę natywną;
- sole metali ciężkich – to związki chemiczne zawierające jony: Hg2+, Pb2+, Ag+, Cd2+ oraz jony innych metali o gęstości większej niż 4,5 g/cm3.
Wszystkie te czynniki powodują rozerwanie wiązań wodorowych, jonowych, mostków disiarczkowych, czyli niszczą wiązania, które stabilizują strukturę łańcuchów polipeptydowych. Choć powszechnie mówi się, że denaturacja jest procesem nieodwracalnym, zgłębiając tajniki chemii, można się dowiedzieć, że w początkowym jego etapie, po usunięciu czynnika denaturującego, może dojść do odtworzenia struktury natywnej białka. Takie zjawisko nazywa się renaturacją. Przykładem denaturacji odwracalnej jest choćby zastosowanie soli amonowych, czego konsekwencją jest usunięcie płaszcza wodnego białka i zmiana jego struktury przestrzennej. Po dodaniu wody, białko wraca do struktury wyjściowej. Czynniki fizyczne prowadzą jednak zawsze do denaturacji nieodwracalnej.
Denaturacja – efekty
Białka, które zostały poddane procesowi denaturacji, posiadają zupełnie inne właściwości fizyczne i chemiczne, czego przyczyną są zmiany w ich strukturze. Oprócz utraty aktywności biologicznej takie białko jest znacznie bardziej podatne na działanie enzymów proteolitycznych oraz zmiany w rozpuszczalności i lepkości.
Denaturacja – przykłady
Denaturacja jest procesem towarzyszącym człowiekowi na każdym kroku, w różnych dziedzinach jego życia. Najczęściej spotyka się ją w kuchni, podczas przyrządzania jajek i innych pokarmów zawierających białka, choć patologiczna denaturacja może również być konsekwencją poparzenia skóry, która w dużej mierze składa się właśnie z białek. Zjawisko denaturacji wykorzystywane jest również w medycynie, aby niszczyć patogenne mikroorganizmy, w szczególności bakteryjne.

 Spirulina w proszku (100% naturalna)
Spirulina w proszku (100% naturalna)Spirulina w proszku to słodkowodna alga, zawierająca duże stężenie witamin, minerałów i innych, ważnych składników odżywczych. Wysoką jakość uzyskano dzięki odpowiednim warunkom klimatycznym, przestrzeganiu restrykcyjnych norm podczas hodowli i …
Zobacz tutaj ...
Bibliografia
- Ptaszek A., Wysalanie i denaturacja białek jaja kurzego oraz żelatyny, Instrukcja do zajęć laboratoryjnych z przedmiotu Chemia Bioorganiczna i Bionieorganiczna.
- Solomons G., Fryhle C., Snyder S., Chemia organiczna, Wydawnictwo PWN, Warszawa 2022.







Zostaw komentarz